- Autor Jason Gerald gerald@how-what-advice.com.
- Public 2023-12-16 11:33.
- Última modificação 2025-01-23 12:43.
A espectrofotometria é uma técnica experimental usada para medir a concentração de um soluto em uma solução específica, calculando a quantidade de luz absorvida por aquela substância. Essa técnica é muito útil porque certos compostos também absorvem diferentes comprimentos de onda de luz em diferentes intensidades. Ao analisar a luz que passa por uma solução, você pode identificar os compostos dissolvidos na solução e suas concentrações. A ferramenta usada para analisar soluções com essa técnica em laboratório é o espectrofotômetro.
Etapa
Parte 1 de 3: Preparando a amostra

Etapa 1. Ligue o espectrofotômetro
A maioria dos espectrofotômetros precisa ser aquecida antes que possam fornecer medições precisas. Então, ligue a máquina e deixe-a descansar por pelo menos 15 minutos antes de medir a amostra.
Use este tempo para preparar a amostra

Etapa 2. Limpe a cubeta ou tubo de teste
Em laboratórios escolares, tubos de ensaio descartáveis podem estar disponíveis, os quais não precisam ser limpos primeiro. No entanto, se você estiver usando uma cubeta normal ou tubo de ensaio, certifique-se de limpar o aparelho completamente antes de usar. Enxágue todas as cubetas com água desionizada.
- Tenha cuidado ao usar cuvetes, pois são muito caras.
- Ao usar a cubeta, não toque no lado por onde a luz passa (geralmente o lado transparente do recipiente).
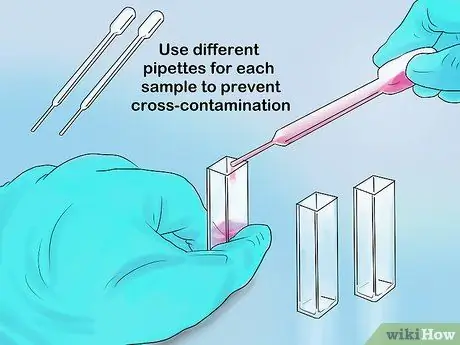
Etapa 3. Despeje amostra suficiente na cubeta
O volume máximo de parte da cubeta é de 1 ml, enquanto o volume máximo do tubo de ensaio é de 5 ml. Suas medições devem ser precisas, desde que a luz do espectrofotômetro ainda possa passar pela amostra e não por uma parte vazia do recipiente.
Se você estiver usando uma pipeta para inserir amostras, use uma nova ponta para cada amostra. Dessa forma, a contaminação cruzada pode ser evitada

Etapa 4. Prepare a solução de controle
Estas soluções, também conhecidas como brancos ou brancos, contêm apenas o solvente na solução a ser analisada. Por exemplo, se você tiver uma amostra de sal dissolvido em água, a solução em branco necessária é água. Se a água que você está usando for vermelha, você também deve usar uma solução branca vermelha. Use um recipiente semelhante para manter a solução em branco no mesmo volume da amostra.

Etapa 5. Limpe a parte externa da cubeta
Antes de inserir a cubeta no espectrofotômetro, certifique-se de que esteja limpa para evitar interferência nas medições devido a partículas de poeira ou impurezas. Use um pano sem fiapos para remover qualquer gota de água ou poeira aderida à parte externa da cubeta.
Parte 2 de 3: Experimentação

Etapa 1. Determine e ajuste o comprimento de onda da luz para analisar a amostra
Use um único comprimento de onda de luz (feixe monocromático) para aumentar a eficácia da medição. Escolha a cor da luz que pode ser absorvida pelo conteúdo químico que se pensa estar dissolvido na amostra de teste. Defina o comprimento de onda de acordo com as especificações do espectrofotômetro que você está usando.
- Em laboratórios escolares, esses comprimentos de onda geralmente serão fornecidos nas instruções experimentais.
- Como a amostra refletirá toda a luz visível, o comprimento de onda da cor da luz experimental geralmente é sempre diferente da cor da amostra.
- Um objeto parece ter uma determinada cor porque reflete um determinado comprimento de onda e absorve todas as outras cores. A grama parece verde porque a clorofila nela reflete o verde e absorve outras cores.
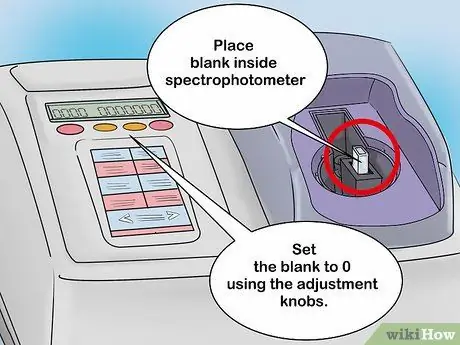
Etapa 2. Calibre o espectrofotômetro com uma solução em branco
Coloque a solução em branco no suporte da cubeta e feche o espectrofotômetro. Na tela do espectrofotômetro analógico, há uma agulha que se move com base na intensidade de detecção da luz. Depois que a solução em branco for inserida, a agulha deve se mover para a direita. Registre esse valor caso precise dele mais tarde. Deixe que a solução em branco permaneça no espectrofotômetro e deslize a agulha até zero usando o botão de ajuste.
- Os espectrofotômetros digitais também podem ser calibrados da mesma maneira. No entanto, esta ferramenta está equipada com uma tela digital. Defina a leitura da solução em branco para 0 com o botão de controle.
- Mesmo que a solução em branco seja removida do espectrofotômetro, a calibração ainda será válida. Portanto, ao medir toda a amostra, a absorbância do branco será automaticamente reduzida.

Etapa 3. Remova o branco e teste os resultados da calibração do espectrofotômetro
Mesmo depois que a solução em branco é removida do espectrofotômetro, a agulha ou número na tela ainda deve indicar 0. Coloque a solução em branco de volta no espectrofotômetro e certifique-se de que a leitura não mude. Se o espectrofotômetro for calibrado corretamente usando uma solução em branco, o resultado na tela ainda deve ser 0.
- Se a agulha ou o número na tela não for 0, repita as etapas de calibração com uma solução em branco.
- Se o problema persistir, procure ajuda ou peça para alguém verificar o espectrofotômetro.

Etapa 4. Meça a absorbância da amostra
Remova a solução em branco e insira a amostra no espectrofotômetro. Aguarde cerca de 10 segundos para que os ponteiros se estabilizem ou os números no visor digital parem de mudar. Registre a porcentagem de transmitância e / ou absorbância da amostra.
- Quanto mais luz é passada, menos luz é absorvida. Normalmente, você precisa registrar o valor de absorbância da amostra, que geralmente é expresso como um número decimal, por exemplo, 0,43.
- Repita a medição de cada amostra pelo menos três vezes e depois calcule a média. Dessa forma, os resultados obtidos serão mais precisos.

Etapa 5. Repita o experimento com diferentes comprimentos de onda de luz
Sua amostra pode conter vários compostos com diferentes absorbâncias dependendo do comprimento de onda da luz. Para reduzir a incerteza, repita as medições da amostra em intervalos de comprimento de onda de 25 nm em todo o espectro de luz. Dessa forma, você pode detectar outros produtos químicos dissolvidos na amostra.
Parte 3 de 3: Analisando Dados de Absorção

Etapa 1. Calcule a transmitância e a absorbância da amostra
A transmitância é a quantidade de luz que pode passar pela amostra e chegar ao espectrofotômetro. Enquanto isso, absorbância é a quantidade de luz absorvida por um dos produtos químicos dissolvidos na amostra. Existem muitos espectrofotômetros modernos que fornecem resultados na forma de transmitância e absorbância. No entanto, se você obtiver um valor de intensidade de luz, também poderá calcular esses dois valores sozinho.
- A transmitância (T) pode ser determinada dividindo a intensidade da luz que passa pela solução de amostra pela quantidade de luz que passa pela solução em branco. Esse valor geralmente é expresso como um número decimal ou uma porcentagem. T = I / I0, onde I é a intensidade da amostra e I0 é a intensidade do branco.
- A absorvância (A) é expressa como um logaritmo de base negativa 10 (expoente) transmitância: A = -log10T. Então, se T = 0, 1, A = 1 (0, 1 é 10 elevado a -1). Isso significa que 10% da luz é passada, enquanto 90% é absorvido. Enquanto isso, se T = 0,01, A = 2 (0,01 é 10 elevado a -2). Isso significa que a luz que é passada é de 0,1%.
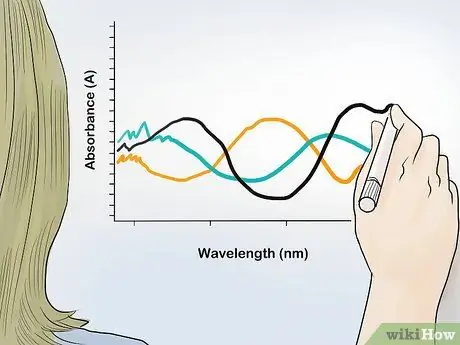
Etapa 2. Represente graficamente o valor da absorbância em função do comprimento de onda
Expresse o valor de absorbância como eixo y e o comprimento de onda como eixo x. A partir dos pontos de todos os resultados de absorbância em cada comprimento de onda, você obterá o espectro de absorbância da amostra e identificará o conteúdo do composto e sua proporção na amostra.
Os espectros de absorção geralmente apresentam picos em determinados comprimentos de onda. Esses comprimentos de onda de pico permitem que você identifique compostos específicos
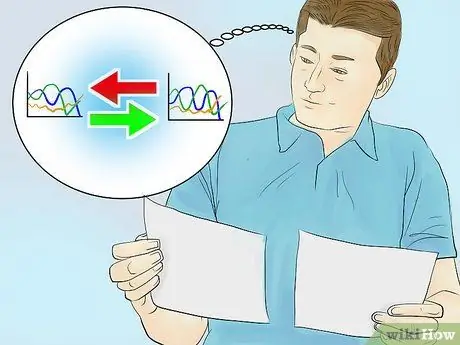
Etapa 3. Compare seu espectro de absorbância com um gráfico de um composto conhecido
Cada composto tem um espectro de absorbância exclusivo e sempre tem o mesmo comprimento de onda de pico em cada medição. Ao comparar o gráfico obtido com o gráfico de um determinado composto conhecido, você pode identificar o conteúdo de soluto na solução de amostra.






